La nitración es
un proceso por el cual se le agrega un grupo nitro a otro compuesto químico
mediante una reacción química. En el caso del benceno, se usa como reactivo una
mezcla de ácido nítrico (HNO3) y ácido sulfúrico (H2SO4).
El H2SO4 libera protones OH- del HNO3 el
cual luego se convierte en agua generando el grupo nitro (NO2+).
Finalmente, el NO2+ es atacado por el benceno
y se produce una reacción de adición electrofílica (se pierde 1 enlace pi para
producir 2 sigma) para recuperar la aromaticidad por la pérdida
de un protón. Así se obtiene el nitrobenceno.
domingo, 31 de marzo de 2013
Propiedades químicas: Halogenación
El cloro y el bromo dan derivados de sustitución que recibe el nombre de harulos de arilo.
C6H6 + Cl2C6H5Cl + HCl
clorobenceno
C6H6 + Br2C6H5Br + HBr
bromobenceno
La halogenacion se favorece por la temperatura baja y por algunos catalizadores, entre esos esta: El hierro o tricloruro de aluminio, que polariza el halogeno para que se produzca de forma energética la reaccion. Los catalizadores mas que todo suelen ser sustancias que presentan deficiencia de electrones.
C6H6 + Cl2C6H5Cl + HCl
clorobenceno
C6H6 + Br2C6H5Br + HBr
bromobenceno
La halogenacion se favorece por la temperatura baja y por algunos catalizadores, entre esos esta: El hierro o tricloruro de aluminio, que polariza el halogeno para que se produzca de forma energética la reaccion. Los catalizadores mas que todo suelen ser sustancias que presentan deficiencia de electrones.
Propiedades físicas del benceno
El benceno (C6H6) es el más simple de los hidrocarburos aromáticos, y el más volátil, líquido a temperatura ambiente. Su punto de fusión es de 5,4° C, y el de ebullición es de 80,1° C. Su densidad es de 0.889 g/cm3 y es insoluble en agua, por lo que al mezclarlo con esta, forma una mezcla heterogénea de dos fases, en la que el benceno se ubica en la parte superior. Es un compuesto altamente tóxico: Su inhalación en grandes cantidades o ingestión puede causar hasta la muerte.
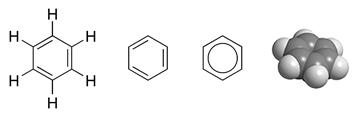 |
| 4 diferentes formas de expresar la molécula de benceno. http://upload.wikimedia.org/wikipedia/commons/6/67/Benzene_structure.png |
Fenol
Su fórmula química es C6H5OH, conocido también como ácido fénico o ácido carbólico y puede sintetizarse mediante la oxidación parcial del benceno. El fenol se emplea para preparar medicamentos, perfumes, fibras textiles artificiales y en la fabricación de colorantes. En aerosol, se utiliza para tratar irritaciones de la garganta. Este fue el primer desinfectante utilizado,pero por su toxicidad ha sido reemplazado por otros menos perjudiciales. El contacto de la piel con cantidades altas de fenol puede producir quemaduras, daño del hígado, orina de color oscuro, latido irregular del corazón y aun la muerte pues en concentraciones altas es venenoso y por ultimo ingerir fenol concentrado puede producir quemaduras internas.
Más usos de los ALQUINOS.
Los alquinos sirven como materia prima en la obtención del metilacetileno que es utilizado en los sopletes porque no se descompone tan fácil como el acetileno y pueden alcanzarse temperaturas mucho más altas; también se utiliza como combustible de cohetes.
Anilina
La anilina,
fenilamina o aminobenceno es un compuesto orgánico que es considerado como la
amina aromática más importante. Este liquido es entre incoloro y un amarillo
muy suave, y tiene un olor muy característico, también es levemente soluble en
agua y se disuelve rápidamente en la mayoría de los solventes orgánicos. Y se puede
producir fácilmente a partir del benceno. La anilina es utilizada para la fabricación
de productos como: manufactura de
perfumes, reveladores de fotografía, producción de colorantes, productos farmacéuticos, fabricación de tintas, desinfectantes, producción de
otros compuestos químicos de tipo orgánico, estabilizadores para la industria
del caucho, herbicidas, barnices y explosivos. La anilina
puede ser tóxica si se ingiere, inhala o por contacto con la piel.
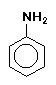
C6H5NH2
http://organica1.org/nomencla/nomen8.htm
http://organica1.org/nomencla/nomen8.htm
Aromaticidad: Criterios geométricos ó estructurales
Uno de los criterios de la aromaticidad son llamados Geométricos ó Estructurales, estos se centran en una de las manifestaciones de la aromaticidad, los cuales son, la igualdad en la longitud de los enlaces y la planaridad de la molécula. La molécula del benceno es plana y todos los enlaces C-C tienen una longitud de 1.3983Å. Sin embargo, se ha atribuido aromaticidad a compuestos no planos.
Inhalación del Butino
Este gas es más pesado que el aire y se acumula en espacios cerrados, particularmente en sótanos y a nivel del suelo. Por este motivo puede causar asfixia en altas concentraciones, ya que este gas causa desplazamiento del aire. Para detectar el gas en estos casos conviene utilizar undetectos de gases específico para el butino.
Solubilidad
Al hablar del benceno se dice que es un líquido incoloro, de olor dulce a escencias. Al referirse a la solubilidad del mismo, se observa que sí es soluble en éter, nafta y cetona. Además, se disuelve en alcohol y en la mayoria de solventes orgánicos.
También, se le conoce como capaz de disolver al yodo y las grasas.
También, se le conoce como capaz de disolver al yodo y las grasas.
Criterios magneticos de aromaticidad de una sustancia
Uno de los criterios empleados para ver la aromaticidad de una sustancia es el magnetismo. En el benceno y en los hidrocarburos se produce una circulación de carga característica en la nube pi, la cual esta en presencia de un campo magnético. La circulación se refleja en el diamagnetismo del compuesto. El diamagnetismo se presenta en todos los sistemas aromáticos en los que haya un anillo de 4n + 2 electrones.
Criterios energéticos de aromaticidad
Están basados en una extensión de la Ley de Hess, según la cual:
1. Los dobles enlaces de un compuesto sufren reacciones independientes. Éstas deben ser isodésmicas y homodésmicas, es decir, que entre ellas se mantenga tanto el número y tipo de enlaces total, como la hibridación de los átomos enlazados.
2. Se llaman "Energía de Estabilización Aromática" a las desviaciones que se observen.
1. Los dobles enlaces de un compuesto sufren reacciones independientes. Éstas deben ser isodésmicas y homodésmicas, es decir, que entre ellas se mantenga tanto el número y tipo de enlaces total, como la hibridación de los átomos enlazados.
2. Se llaman "Energía de Estabilización Aromática" a las desviaciones que se observen.
Teoría orbitales moleculares en la estructura dle benceno
Los átomos de carbono del benceno presentan hibridación 3 sp2 y 1 p puro. Estos forman orbitales moleculares σ, al enlazarse entre C-C por medio de enlaces C(sp2)-C(sp2), y entre C-H por medio de enlaces C(sp2)-H(s). Además, tienen un orbital perpendicular p que se enlaza con el del carbono contiguo. Por el solapamiento por arriba y por debajo del plano molecular, se crean 6 orbitales moleculares π. Estos dan pie a un círculo de densidad electrónica que es representado como una circunferencia dentro del anillo o hexágono del benceno.
Consultada la imagen en: http://es.wikipedia.org/wiki/Aromaticidad
Teoría de la resonancia para la estructura del benceno
Aromáticos: Estructura Propuesta por Kekule

Después de observar los resultados de las reacciones del benceno cuando se tenían los isómeros de los productos monoderivados y derivados , explicó que existen dobles enlaces alternados y que se forma una nube de electrones π por encima y debajo del anillo de 6 carbonos.
Dato curioso: Alquinos con actividad fisiológica
Se ha descubierto un raro ejemplo en el que se encuentran alquinos en moléculas biológicas. Al aislar compuetos naturales que contienen alquinos de los microbios, se obtiene que estos compuestos tienen una gran actividad antibacteriana y anticancerosa. Lastimosamente, estos pueden ser muy tóxicos hacia los mamíferos para ser utilizados como farmacéuticos.
Que son los aromaticos?
Son hidrocarburos caracterisados por presentanr al menos una cadena cerrada, tambien llamados cíclicos. El aromatico mas simple es el benceno (C6H6). Anteriormente, la palabra aromatico solo se referia a un producto del alquitrán mineral, el benceno, y a sus derivados. Sin embaro, en la actualidad este termino incluye casi a la mitad de todos los compuestos orgánicos; el resto son los llamados compuestos alifáticos.
CUARTA
ASIGNACIÓN
LEA CUIDADOSAMENTE LA FORMA COMO
DEBERÁ HACER SU PARTICIPACIÓN EN ESTA ASIGNACIÓN.
EN ESTA OCASIÓN LAS PARTICIPACIONES
DEBERÁN HACERSE EN ORDEN DE LOS TEMAS, ES DECIR SI USTED HACE LA PRIMERA
ENTRADA ESTA DEBERÁ SER ACERCA DE LA DEFINICIÓN GENERAL DEL GRUPO, SI HACE LA
SEGUNDA ENTRADA DEBERÁ HABLAR DE LA ESTRUCTURA PROPUESTA POR KEKULE, Y ASÍ
SUCESIVAMENTE HASTA LLEGAR A LAS FORTALEZAS Y DEBILIDADES DEL GRUPO.
Si su entrada no sigue el orden de
los temas quedará anulada inmediatamente.
Los temas son:
Ø Definición general (sin estructura)
origen del nombre “aromático”
Ø Estructura propuesta por Kekule
Ø Teoría de la resonancia para la
estructura del benceno
Ø Teoría de los orbitales moleculares
para la estructura del benceno
Ø Criterios de aromaticidad de una
sustancia
Ø
Propiedades
físicas, recuerden que hay muchas propiedades físicas
Ø
Propiedades
químicas, lo mismo que las físicas, el benceno presenta varias reacciones.
Ø
Obtención: ya sea de fuentes naturales o por
reacciones de compuestos químicos.
Ø Origen histórico: cuando
lo empezaron a usar, cual fue el primer producto de la familia en usarse.
Ø Usos generales y
productos destacados por su abundancia, usos, por los retos de contaminación
que involucra, por su importancia en la economía, etc.
Ø Proyecciones en la
innovación de productos.
Ø Impacto ambientales que
suponen la fabricación o uso de estas sustancias, tanto para el medio ambiente
como para la salud humana.
Ø Fortalezas y debilidades
del grupo funcional
FLASH
INFORMATIVO 2
Deben leer las instrucciones de cada nueva asignación antes de hacer las entradas. Si no se siguen las instrucciones dadas la entrada se anulará y quedarán sin puntos para la participación de ese grupo funcional en particular.
Como les indique anteriormente deben leer las entradas de las otras compañeras para hacer sus participaciones. No sirve ver los títulos de las entradas que aparecen a mano derecha de la pantalla, ya que de un solo tema se pueden hacer entradas con enfoques o datos distintos, o al contrario el titulo no esta muy bien puesto y repiten los datos.
Deben leer las instrucciones de cada nueva asignación antes de hacer las entradas. Si no se siguen las instrucciones dadas la entrada se anulará y quedarán sin puntos para la participación de ese grupo funcional en particular.
Como les indique anteriormente deben leer las entradas de las otras compañeras para hacer sus participaciones. No sirve ver los títulos de las entradas que aparecen a mano derecha de la pantalla, ya que de un solo tema se pueden hacer entradas con enfoques o datos distintos, o al contrario el titulo no esta muy bien puesto y repiten los datos.
1-BUTINO
Este alquino también es conocido como etilacetileno o simplemente butino. A temperatura ambiente, su estado es gaseoso. En estado puro es incoloro, y en concentraciones muy altas suele presentar un olor a ajo. Este es extremadamente inflamable y reactivo, por lo que se emplea en la síntesis de otros compuestos orgánicos. Su formula molecular es C4H6, y su formula estructural es:
 |
| http://compuestosorganicos201.blogspot.com/2012/06/alquinos.html |
sábado, 30 de marzo de 2013
Acidez del Etino
El acetileno es más ácido que el etano y el eteno, a causa del orbital en el que se ubica el par de electrones libres de su base conjugada cuando libera H+. Mientras que los e- del anión vinilo -base conjugada del eteno- se encuentran en un orbital de sp2 (33% de carácter s), los del anión acetiluro -base del acetileno- están en el sp (50% de carácter s), por lo tanto este último los atrae con mayor fuerza, provocando que sea menos básico que el Eteno por estar menos presto a ceder sus e- (definición de bases según Lewis), y éste a su vez menos básico que el Etano, con sus e- en el orbital sp3 (25% de carácter s).
 |
| http://ocwus.us.es/quimica-organica/quimica-organica-i/temas/7_alquinos/leccion15/pagina_05.htm |
FLASH INFORMATIVO
A partir del siguiente grupo funcional, las entradas que hablen de reacciones generales o particulares de los grupos, que no incluyan la reacción escrita con ecuaciones y formulas químicas será anulada y por lo tanto para esa asignación no se le sumarán puntos a la estudiante. Lo mismo ocurrirá cuando hablen de un producto como poetas y no como químicos, estos últimos hablan con formulas químicas donde aparecen los simbolos de los elementos.
Cuando se solicite repetir una entrada, no se debe hacer sobre la entrada a reemplazar, sino hacer una nueva.
Cuando se solicite ampliar el contenido de una entrada, se debe hacer sobre la misma entrada y me deben avisar por cibercolegios para volverla a revisar.
A partir del siguiente grupo funcional, las entradas que hablen de reacciones generales o particulares de los grupos, que no incluyan la reacción escrita con ecuaciones y formulas químicas será anulada y por lo tanto para esa asignación no se le sumarán puntos a la estudiante. Lo mismo ocurrirá cuando hablen de un producto como poetas y no como químicos, estos últimos hablan con formulas químicas donde aparecen los simbolos de los elementos.
Cuando se solicite repetir una entrada, no se debe hacer sobre la entrada a reemplazar, sino hacer una nueva.
Cuando se solicite ampliar el contenido de una entrada, se debe hacer sobre la misma entrada y me deben avisar por cibercolegios para volverla a revisar.
Tautomería
La tautomería
es el reajuste rápido y reversible que sufre una molécula. Esto se aplica a una
migración protónica intramolecular de forma reversible. Se podría considerar
como una reacción ácido-base, en donde una parte de la estructura es el ácido (libera
el protón) y la otra la base (acepta el protón). Finalmente, a las estructuras
resultantes se les llama tautómeros y por el hecho de ser reversible se produce
una equilibro, donde la constante que busca la estabilidad del compuesto recibe
el nombre de constante tautomérica Kt.
viernes, 29 de marzo de 2013
Hidratación de alquinos
La hidratación de alquinos puede llevarse a cabo con H2SO4 acuoso con la presencia de un catalizador como las sales mercúricas (HgSO4). Esta reacción se da por la utilización de ácido sulfúrico acuoso como un medio de reacción y como catalizador se utiliza sulfato de mercurio (II) u óxido de mercurio (II). En ocasiones se requiere agregar un co-disolvente como el metanol o ácido acético para solubilizar el alquino principal.
Gracias a esta reacción se forma un alcohol especial ya que este consta de un grupo hidroxilo sobre un carbono de un doble enlace. Estos alcoholes reciben el nombre de "enoles" y se isomerizan con gran rapidez a los aldehídos o cetonas bajo condiciones utilizadas en la reacción, este proceso se conoce como tautomería ceto-enólica.
Gracias a esta reacción se forma un alcohol especial ya que este consta de un grupo hidroxilo sobre un carbono de un doble enlace. Estos alcoholes reciben el nombre de "enoles" y se isomerizan con gran rapidez a los aldehídos o cetonas bajo condiciones utilizadas en la reacción, este proceso se conoce como tautomería ceto-enólica.
Anticonceptivos
Un ejemplo de los alquinos en la medicina se da en los anticonceptivos. El etinil-estradiol es una hormona femenina sintética, ingrediente de las píldoras anticonceptivas. La fabricación de la pastilla anticonceptiva consiste en la combinación de un estrógeno derivado del estradiol (hormona esteroide sexual femenina que con la progesterona esta encargada de la maduración, liberación y mantenimiento de un óvulo fertilizado en el útero) y una progestina (estrógeno sintético con características similares a la progesterona pero que en combinación con el estradiol funciona como anticonceptivo). La sustitución del carbono 17 con un grupo etinil le da al estradiol resistencia a la degradación del hígado, y esto permite que se puedan fabricar píldoras, es decir, que se produzcan estos anticonceptivos por métodos orales.
Imágenes:
http://www.blogodisea.com/2010/testosterona-estradiol-similares-diferentes/cuerpo-humano/
http://www.carlaantonelli.com/foros/viewtopic.php?f=29&t=10797&start=135
Imágenes:
http://www.blogodisea.com/2010/testosterona-estradiol-similares-diferentes/cuerpo-humano/
http://www.carlaantonelli.com/foros/viewtopic.php?f=29&t=10797&start=135
Uso: iluminación
En el siglo XIX, las lámparas de acetileno gaseoso se comenzaron a usar en el alumbrado público. Dentro de la lámpara se producía acetileno de la reacción entre carburo de calcio y agua. Con el fin de la Primera Guerra Mundial, se dejaron de usar como alumbrado público. Sin embargo, hoy en día se utilizan para la iluminación de lugares con poca iluminación, como las cuevas, debido a que ofrecen una ilumnicación más brillante que la eléctrica. Además, indican el nivel de oxígeno presente puesto que las llamas de estas lámparas se producen de la combustión del acetileno.
Lámparas que se usaban anteriormente
Consultado en: http://aguito.madteam.net/articulos/2007-04/acetileno-luz-en-la-oscuridad/
Impacto ambiental del PVC
Al
fabricar PVC, la sal tradicional se convierte en gas cloro y compuestos
organoclorados. Esta producción
de gas cloro y de etileno gasta mucha energía. Así sucede en Alemania, donde la
producción de cloro representa el 25% de
la energía consumida por las fábricas. Por otra
parte, la elaboración de cualquier compuesto organoclorado trae consigo residuos.
En este caso, los residuos de PVC contienen niveles de dioxinas de hasta 214
partes por billón, éstas constituyen un
grupo de compuestos químicos que son contaminantes ambientales.
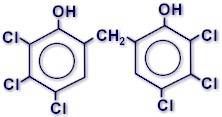
Hexaclorofeno, ejemplo de compuesto organoclorado. (Compuesto en el cual los átomos de hidrógeno son reemplazados por átomos de cloro).
Consultado en: http://parasitipedia.net/index.php?option=com_content&view=article&id=314&Itemid=407

Hexaclorofeno, ejemplo de compuesto organoclorado. (Compuesto en el cual los átomos de hidrógeno son reemplazados por átomos de cloro).
Consultado en: http://parasitipedia.net/index.php?option=com_content&view=article&id=314&Itemid=407
Alquilación de alquinos
Los alquinos terminales son aquellos que presentan hidrógenos ácidos en su estructura. Gracias a la acidez del H en estos alquinos, se pueden sintetizar utilizando bases fuertes que desprendan ese ácido. De esta manera, al reaccionar con una de ellas se forman acetiluros (base conjugada del alquino). Esta síntesis, llamada alquilación, tiene lugar en dos etapas que se pueden observar a continuación:




Nota: Para que se produzca la reacción es necesario utilizar haloalcanos primarios.
Polímeros polialquinos
Los alquinos generan polímeros los cuales son llamados polialquinos. Estos, son semiconductores orgánicos y aunque son materiales flexibles, están dotados parecido al silicio (constituye un 28% de la corteza terrestre y se forma de pequeños atomos dotados de carga eléctrica). Los polímeros son macromoléculas que se forman por la unión de monómeros (moléculas más pequeñas). En la vida cotidiana del hogar se utilizan estos solventes orgánicos como agentes para la limpieza a seco, quitamanchas y diluyentes de pintura. También sirven de limpiadores de escritorios y como removedores de cera.
Suscribirse a:
Comentarios (Atom)







