ASPAEN
GIMNASIO CARTAGENA DE INDIAS
QUÍMICA:
ALCOHOLES
PRESENTADO A:
MARÍA CECILIA ESTRADA
PRESENTADO POR:
ARIELLA BARBOZA
MARÍA ALEJANDRA MONROY
VALERIA ESPITIA
NATHALIE ARAÚJO
10 DE MAYO DE 2013
·
Definición
Alcoholes son compuestos químicos orgánicos que tienen un grupo hidroxilo (-OH) en su estructura en sustitución de un átomo
de hidrógeno, el cual esta enlazado con un átomo de carbono.
·
Estructura de los
alcoholes

Existen tres tipos de alcoholes, los alcoholes primarios, en el que un átomo de hidrogeno, sustituido por un
OH, pertenece a un carbón primario. Los segundos son los alcoholes secundarios,
donde el átomo de hidrogeno es sustituido por un OH que pertenece a un carbón
secundario. Por último, un alcohol terciario es en el que el átomo de hidrogeno
sustituido por un OH pertenece a un carbón terciario.
·
Propiedades
físicas
Solubilidad
Debido a que el alcohol
tiene un grupo OH en su estructura, estos forman puentes de hidrogeno, lo que
los hace solubles en agua. Pero a mayor cantidad de hidrogeno, esta solubilidad
va desapareciendo. A partir del hexanol, el alcohol se torna aceitoso, ya que
la parte polar de la molécula se hace muy pequeña en comparación con la porción
hidrocarburo.

·
Punto de ebullición:
Para los alcoholes, esta
propiedad es proporcional a la polaridad del compuesto y a la cantidad de puentes
de hidrogeno en la estructura. Esto se debe a que los puentes de hidrogeno
hacen que los puntos de ebullición sean mucho mas altos que los de los
hidrocarburos con su mismo peso molecular, ya que los puentes de hidrogeno son más
difíciles de romper.


·
Punto de fusión:
Presenta el mismo
comportamiento que el punto de ebullición, aumenta a medida que aumenta el número
de carbonos.


·
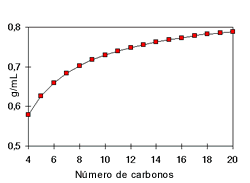
Densidad:
Aumenta conforme aumenta
el número de carbonos y las ramificaciones de las moléculas. Esto se debe a que
las atracciones entre las moléculas son más fuertes, como resultado de la alta
cantidad de carbonos que se atraen, lo cual hace que las moléculas estén más
unidas, y por ello su densidad aumente.

·
Propiedades
químicas
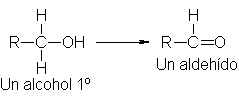
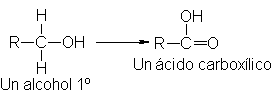
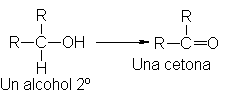
Oxidación:
La oxidación es la
reacción de alcoholes disminuyen el numero de enlaces C-H o aumenta el número
de enlaces C-O para producir ácidos carboxílicos, cetonas o aldehídos
dependiendo del tipo de alcohol y de catalizador.
Deshidrogenación:
Los alcoholes primarios
y secundarios cuando se calientan en contacto con ciertos catalizadores,
pierden átomos de hidrógeno para formar aldehídos o cetonas. Si esta
deshidrogenación se realiza en presencia de aire (O2), el hidrógeno
sobrante se combina con el oxígeno para dar agua.

Halogenacion:
El alcohol reacciona con
un ácido para formar haluros de alquilo más agua.
Tomado de: http://organicaudla3.wikispaces.com/Hidrocarburos+Insaturados
Deshidratación:
Es una propiedad de los
alcoholes mediante la cual podemos obtener alquenos, en esta reacción de
eliminación donde el alcohol pierde su grupo OH para dar origen a un alqueno,
podemos observar el carácter básico de los alcoholes.


·
Obtención:
Natural:
Algunos alcoholes como el etanol,
pueden ser producidos por fermentacion alcoholica de granos o y frutas con
levadura, este ultimo lo encontramos en forma de combustible o bebida. Incluso,
este tipo de alcohol puede ser producido en casa, por medio de la destilacion
de la caña de azúcar fermentada.
Industrial:
·
Origen histórico: cuando lo empezaron a usar, cual
fue el primer producto de la familia en usarse.
La palabra alcohol resulta del árabe الكحول al-kukhūl 'el espíritu', de al-y kuḥūl que significa 'sutil'. En la
antigüedad, se llamaba "espíritu" a los alcoholes: “espíritu de vino"
al etanol, y "espíritu de madera" al metanol.
Los árabes descubrieron el alcohol extraído del vino por
destilación. No obstante, se descubre en el siglo XVI por Arnau de Villanova, alquimista y profesor de medicina. La quinta esencia de Ramon Llull no era otra cosa que el
alcohol rectificado a una temperatura más baja. Además, Lavoisier dio a conocer el origen y
la manera de producir el alcohol con la fermentación vínica, el demostró que
con la atribución de levadura de cerveza, el azúcar de uva se convierte en
acido carbónico y alcohol.
·
Usos generales y
productos destacados por su abundancia, usos, por los retos de contaminación
que involucra, por su importancia en la economía, etc.
Diariamente encontramos el alcohol, casi
en todos los productos que utilizamos. El más destacado por su abundancia es el
alcohol etílico, ya que las grandes y pequenas industrias lo utilizan como
disolvente para pinturas, barnices, condimentos, lacas, perfumes, productos de
limipieza, etc.
Otro alcohol es el alcohol alilico,
el cual es el segundo compuesto alilico mas importante de la industria. Este se
utiliza principalmente en la fabricacion de productos farmaceuticos y en
sintesis quimicas.
El alcohol obtenido a partir de la
fermentacion de frutas, es utilizado como bebida, como vinos, cervezas, vodka,
entre otras. Estos ultimos productos, han ocasionado un impacto favorable para
la economia pero no tanto para la sociedad, debido a que causa desinhibicion en
el sistema nervioso de las personas.
·
Proyecciones de
innovación
El etanol como
combustible:
El etanol es una
alternativa de combustible para el futuro, es limpio, renovable y su emisión de
gas carbónico es reducida. Puede sustituir a la gasolina en motores especiales,
o ser mezclado con ella en motores convencionales. También se lo adiciona a
aceites vegetales refinados en la producción de biodiesel.
Es utilizado en
heladerías como ingrediente para la preparación de las paletas. Tomado de: http://www.s1ngular.com/innovadores-helados-con-alcohol/
·
Impacto ambientales
que suponen la fabricación o uso de estas sustancias, tanto para el medio
ambiente como para la salud humana.
Riesgos
para la salud humana:
Se
da la intoxicación por alcohol metílico en las cuales las consecuencias o
posibles síntomas son los siguientes: irritación de las mucosas, cefalea,
zumbido de oídos, vértigo, insomnio, nistagmo. Por otra parte, pueden
producirse lesiones cutáneas por la acción irritante y disolvente del alcohol
metílico y también por la acción lesiva de los tintes y resinas disueltas en
él.
Por
otro lado, el consumo excesivo de alcohol etílico puede causar la pérdida de
memoria y promueve la ocurrencia de un paro cardiaco.
Además,
Un riesgo industrial se debe a la exposición a vapores en un lugar donde se
utiliza alcohol etílico. La exposición a concentraciones superiores a 5.000 ppm
causa irritación de los ojos y la nariz, cefalea, sopor, fatiga y narcosis. El
alcohol no oxidado se excreta en la orina y en el aire espirado, de manera que
apenas se producen efectos acumulativos
Riesgos
para el medio ambiente:
Aunque sea menos contaminante que la gasolina, este
siguen contaminando el medio ambiente ya que toda combustión contamina.
·
Fortalezas y
debilidades del grupo funcional
Fortalezas
|
Debilidades
|
Es conocido como el combustible de mayor
disponibilidad. Además, se lleva a cabo una combustión más limpia que en el
caso de la gasolina.
|
Es toxico cuando se consume una gran
cantidad, por ejemplo, de alcohol etílico.
|
Es usado como disolvente en fármacos y
perfumes.
|
|
Es usado para emergencias ya que se el alcohol
de botiquín está compuesto en su mayor parte de alcohol etílico.
|

Bonita tarde;
ResponderEliminarBuena información, mala presentación, pero muy entendible.
Gracias.
abril "....."
ResponderEliminarque buen nombre XD